
العسل هو عامل قديم لتبديل الجرح الطبيعي وقد أعيد تقديمه إلى رعاية الجروح السريرية الحديثة لأنه يحتوي على العديد من النشاط الحيوي. في هذه الدراسة ، تم دمج العسل في غشاء نانوفيون النانوي القائم على الجينات/PVA لتطوير مادة خلع الجرح فعالة. وقد لوحظت التشكل والتكوين الكيميائي للغشاء الليفي النانوي عن طريق مسح المجهر الإلكتروني وتوصيفه عبر التحليل الطيفي للأشعة تحت الحمراء ، على التوالي ، مما يدل على أن العسل قد تم إدخاله بنجاح إلى ألياف النانو. أظهرت الأغشية الليفية النانوية مع زيادة محتوى العسل نشاطًا معززًا مضادات الأكسدة ، مما يشير إلى القدرة على التحكم في الإفراط في إنتاج أنواع الأكسجين التفاعلية. أثبت مقايسة انتشار القرص وفحص الاتصال الديناميكي النشاط المضاد للبكتيريا للألياف النانوية المحملة بالعسل باتجاه البكتيريا إيجابية الجرام (المكورات العنقودية الذهبية) والبكتيريا سالبة الجرام (Escherichia coli). يوضح اختبار السمية الخلوية السمية والتوافق الحيوي للأغشية الليفية النانوية. لذلك ، فإن الأغشية العسل/الجينات المتقدمة/PVA نانوفيفيات واعدة لضمادات الجرح.
يلعب الجلد دورًا مهمًا في حماية الجسم من التدخلات البيئية الخارجية مثل مسببات الأمراض والمواد الكيميائية (Chua et al. ، 2016). بمجرد أن يكون هيكل أو وظيفة الجلد معيبًا ، يكون الجسم عرضة للغزو الميكروبي وعدوى الجرح ، والذي يؤخر التئام الجروح ويمكن أن يكون مهدد الحياة (Unnithan ، Gnanasekaran ، Sathishkumar ، Lee ، & Kim ، 2014). خلع الجرح هو طريقة فعالة وشائعة لتعزيز التئام الجروح. الضمادات التقليدية ، مثل القطن والشاش ، لها مزايا منخفضة التكلفة وقدرة امتصاص عالية. ومع ذلك ، فإنهم يلعبون دورًا سلبيًا فقط في عملية الشفاء من خلال عزل الجرح عن الملوثات (Mele ، 2016 ؛ Pilehvar-Soltanahmadi et al. ، 2018). علاوة على ذلك ، فإن الجفاف ، والتصاق المعزز على الجرح ، نتيجة للضمادات التقليدية ، يتسبب في عدم الراحة والألم للمريض وكذلك تأخير التئام الجروح (Mayet et al. ، 2014). يجب أن يكون لخلع الجرح المثالي ، من ناحية ، هيكلًا مقابلًا يمنع الغزو الميكروبي ويسمح للتبادل الغازي (Jayakumar ، Prabaharan ، Sudheesh Kumar ، Nair ، & Tamura ، 2011). من ناحية أخرى ، يجب أن تكون مواد الملابس متوافقة حيوياً ، وتمتص الإفرازات الزائدة ، وتمتلك خصائص نشطة حيوياً لتعزيز التئام الجروح ، مثل السلوك المضاد للبكتيريا وإمكانية مضادات الأكسدة (Chhatri et al. ، 2011 ؛ Naseri-Nosar & Ziora ، 2018) .
تم استكشاف إنشاءات مختلفة من ضمادات الجروح لتسهيل التئام الجروح ، مثل الإسفنج ، والهيدروجيلز ، والهيدروكولويد ، والأفلام (Simões et al. ، 2018). من بين هؤلاء ، يمتلك غشاء electrospun nanofibrous بنية داعمة ثلاثية الأبعاد ، وحجم مسام صغير ، ونسبة عالية من السطح إلى الحجم ، والتي تم الإبلاغ عن إمكانية إمكانية كبيرة كضمادات جرحية (Abdelgawad ، Hudson ، & Rojas ، 2014). يمكن أن يحاكي البنية الداعمة ثلاثية الأبعاد هيكل المصفوفة الطبيعية خارج الخلية ، والتي تفضي إلى نمو الخلايا والالتصاق والانتشار (Zhang ، Oh et al. ، 2017). يمكن أن يسهل حجم المسام الصغير والمسامية العالية للحصيرة الليفية النانوية التبادل الغازي والعزلة البكتيرية أثناء إصلاح الجرح (Chui ، Moutuy ، & ye ، 2018). ثبت أن نسبة الألياف النانوية العالية من الألياف النانوية مفيدة لتحميل وتسليم الأدوية لاستعادة الجروح (Sill & Recum ، 2008 ؛ Zhang ، Lim ، Ramakrishna ، & Huang ، 2005).
تم استخدام العديد من المواد كمواد كهربائية ، من بينها البوليمرات الطبيعية ، أظهرت مزايا مختلفة لتطبيق إصلاح الجروح ، مثل الماء ، وعدم التسمم والمساعدة للالتصاق بالخلايا وانتشاره (Hsu et al. ، 2004). الجينات ، باعتبارها بوليمر طبيعي ، هي عديد السكاريد الأنيوني الذي لديه توافق حيوي ممتازة وقابلية التحلل الحيوي (Coşkun et al. ، 2014). علاوة على ذلك ، يمكن أن تمتص الجينات الكفاءة الإفراز الزائد بكفاءة وتوفر بيئة رطبة أثناء عملية التئام الجروح بسبب ارتفاعها في الماء (Coşkun et al. ، 2014 ؛ Summa et al. ، 2018). ومع ذلك ، يصعب على electrospin alginate النقي بسبب الموصلية الكهربائية العالية ، والتوتر السطحي العالي (Xiao & Lim ، 2018) وعدم وجود تشابكات سلسلة من محلولها المائي (Li et al. ، 2013). لذلك ، تمت إضافة البوليمرات الاصطناعية مثل كحول البوليفينيل (PVA) ، لزيادة قابلية الكهربية بالإضافة إلى القوة الميكانيكية للجينات (Shen & Hsieh ، 2014) ، في حين تم تحديد PVA أيضًا على أنها مادة خلع جراحية مواتية (Fu et al. ، 2016 ؛ Zhou et al. ، 2008).
للحصول على تأثير أفضل للشفاء ، تمت دراسة الضمادات الليفية النانوية المدمجة مع العوامل المضادة للبكتيريا ، مثل الجسيمات النانوية الفضية وأكسيد المعادن والمضادات الحيوية ، (Liu et al. ، 2018 ؛ Mokhena & Luyt ، 2017 ؛ Shalumon et al. ، 2011) . تم استخدام العسل ، بسبب مضادات البكتيريا (Martinotti & Ranzato ، 2018) ، ومضادات الالتهابات ، ومضادات الأكسدة (Bertoncelj ، و Doberšek ، و Jamnik ، و Golob ، 2007) ، في رعاية الجرح التي تعود إلى 2000 قبل الميلاد (Minden-Birkenmaier & Bowlin ، 2018). كما تم الإبلاغ عن إظهار القليل من السمية على الخلايا الليفية وزيادة معدل إعادة الظهارة (Ranzato ، Martinotti ، & Burlando ، 2012). Ranzato et al. أظهر أن العسل سهل الإغلاق الجرح (رانتساتو ، مارتينوتي ، وبورلاندو ، 2013). في الآونة الأخيرة ، تم دمج العسل في البوليمرات المختلفة عن طريق الكهربي ، مثل الحرير الأليفية ، PVA و Chitosan (Sarhan & Azzazy ، 2015 ؛ Sarkar ، Ghosh ، Barui ، & Datta ، 2018 ؛ Yang et al. ، 2017).

الشكل 1. العسل/SA/PVA الألياف النانوية ملفقة بواسطة electrospinning. (أ) توضيح تخطيطي
من تحضير الحل وعملية electrospinning. (ب) صورة للعسل/SA/PVA
غشاء النانو.
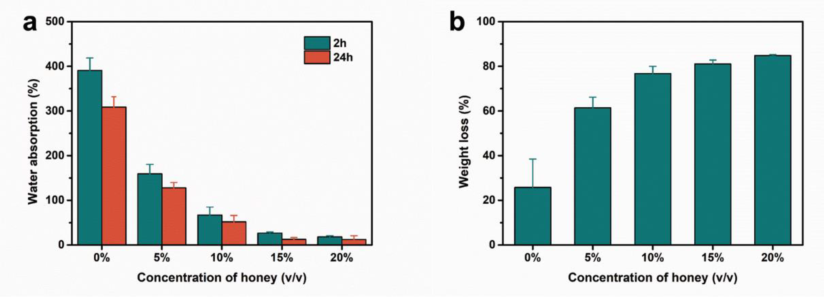
الشكل 2. امتصاص الماء (أ) وفقدان الوزن (ب) من أغشية الألياف النانوية العسل/SA/PVA
مع اختلاف محتوى العسل: 0 ٪ ، 5 ٪ ، 10 ٪ ، 15 ٪ ، و 20 ٪. النتائج تعني ± SD (ن = 3).
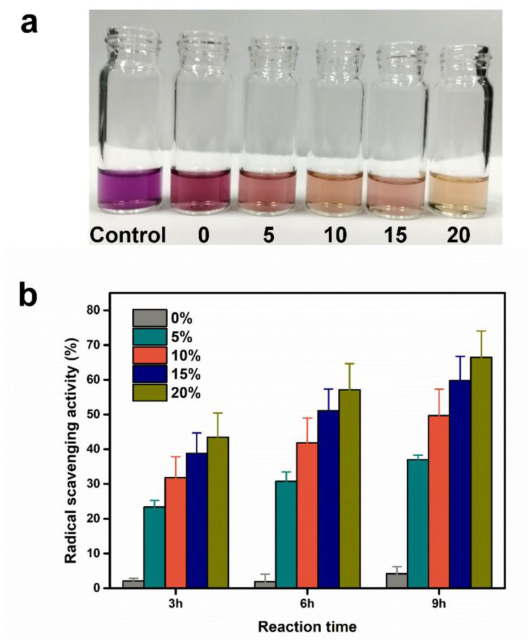
الشكل 3. النشاط المضاد للأكسدة من أغشية الألياف النانوية العسل/SA/PVA. (أ) صور
حلول DPPH بعد رد الفعل مع أغشية ألياف النانو التي تحتوي على محتوى عسل مختلف
(0 ٪ ، 5 ٪ ، 10 ٪ ، 15 ٪ ، و 20 ٪) لمدة 9 ساعات. (ب) نشاط الغزو الراديكالي DPPH من الألياف النانوية
مدمجة مع محتوى عسل مختلف (0 ٪ ، 5 ٪ ، 10 ٪ ، 15 ٪ ، و 20 ٪). النتائج تعني ±
SD (ن = 3).
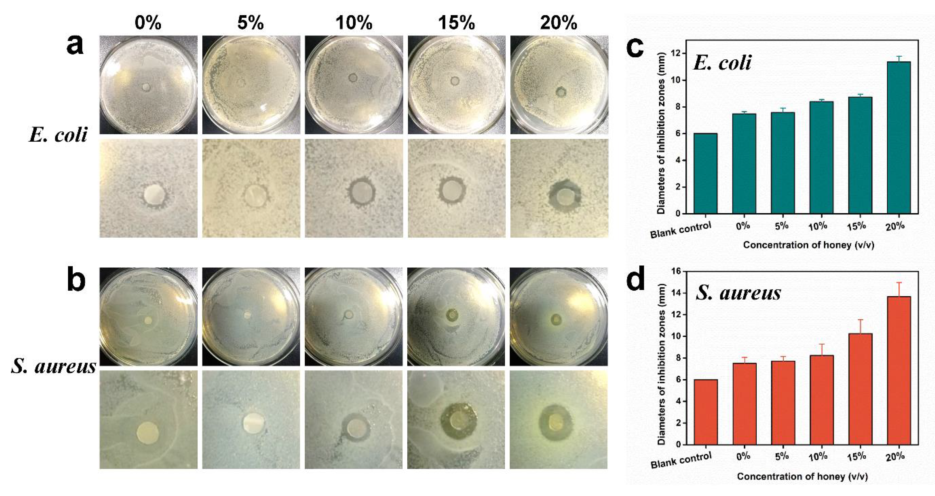
الشكل 4. النشاط المضاد للبكتيريا من الأغشية النانوية النانوية النانوية العسل/SA/PVA مع
تم تقييم محتوى العسل المتغير (0 ٪ ، 5 ٪ ، 10 ٪ ، 15 ٪ ، و 20 ٪) عن طريق اختبار انتشار القرص. (AB)
صور منطقة تثبيط ضد E. coli (A) و S. aureus (B). (CD) حجم
منطقة تثبيط ضد E. coli (C) و S. aureus (D). النتائج تعني ± SD (ن = 3).
مراجع
1.Tang Y ، Lan X ، Liang C ، et al. غشاء الجينات المحملة العسل/PVA النانوي النانوي مثل خلع الجرح النشطة بيولوجيًا محتملاً [J]. البوليمرات الكربوهيدرات ، 2019 ، 219: 113-120.
